Kalor berbeda dengan suhu, walaupun
keduanya memiliki hubungan yang sangat erat. Suhu adalah derajat panas atau
dingin suatu benda, sedangkan kalor adalah energi yang dipindahkan dari suatu
benda ke benda yang lain. Suhu dan kalor dapat dibedakan dengan jelas pada
peristiwa perubahan wujud zat. Untuk mengubah es menjadi air diperlukan kalor.
Pada peristiwa perubahan wujud ini, es bersuhu 00C berubah menjadi
air bersuhu 00C. Jadi tidak ada perubahan suhu pada es mencair,
tetapi dibutuhkan kalor untuk mengubah wujud es tersebut.
Besar kecilnya kalor yang dibutuhkan
suatu benda(zat) bergantung pada 3 faktor :
1.
massa zat
2.
jenis zat (kalor jenis)
3.
perubahan suhu
Sehingga secara matematis dapat dirumuskan :
Dimana:
Q = kalor yang dibutuhkan (J)
m = massa benda (kg)
c = kalor jenis (J/kg oC)
= (T2- T1) = perubahan
suhu (oC)
Satuan Kalor dan Tara
Kalor Mekanik
Satuan kalor adalah kalori (disingkat
kal). Kalori adalah jumlah kalor yang diperlukan untuk menaikan suhu 1 gram air
sebesar 1 oC (tepatnya dari 14,5 oC menjadi 15,5 oC).
Jumlah kalor yang diperlukan berbeda-beda untuk suhu air yang berbeda. Untuk
jumlah kalor yang sama, kenaikan suhu air sebesar 1 oC hanya terjadi
antara suhu 14,5 oC sampai 15,5 oC. Satuan kalor yang sering digunakan, terutama
untuk menyatakan nilai energi makanan adalah kilokalori (kkal). 1 kkal = 1000
kalori. Nama lain dari 1 kkal = 1 Kalori (huruf K besar). Satuan kalor untuk
sistem Bristish adalah Btu (British thermal unit = satuan termal Inggris). 1
Btu = jumlah kalor yang diperlukan untuk menaikkan suhu 1 pound air sebesar 1 oF
(Tepatnya dari 63 oF menjadi 64 oF) .
Kalor berkaitan dengan energi karenanya
kita perlu mengetahui hubungan antara satuan kalor dengan satuan energi.
Berdasarkan percobaan yang dilakukan oleh Joule dan ilmuwan lainnya, diketahui
bahwa usaha sebesar 4,186 Joule setara dengan 1 kalori kalor.
1 kalori = 4,186 Joule
1 kkal = 1000 kalori = 4186 Joule
1 Btu = 778 ft.lb = 252 kalori = 1055 Joule
(1 kalori = 4,186 Joule dan 1 kkal = 4186 disebut tara kalor
mekanik)
Kapasitas Kalor
dan
Kalor
Jenis
Kapasitas kalor adalah banyaknya kalor
yang diperlukan untuk menaikkan suhu seluruh benda sebesar 1 derajat celcius.
Keterangan : C = kapasitas kalor, Q = banyaknya kalor,
T= perubahan suhu.
Kalor jenis adalah banyaknya kalor yang
dibutuhkan untuk menaikkan suhu 1 kg zat sebesar 1 derajat celcius. Alat yang
digunakan untuk menentukan besar kalor jenis adalah kalorimeter.
Keterangan: c = kalor jenis (J/kg oC), Q = banyaknya
kalor, m = massa benda (kg),
= perubahan suhu (oC)
Asas Black
Jika kita mencampur air panas dan dingin didalam
suatu wadah terbuka, maka akan terjadi perpindahan kalor dari air panas menuju
air dingin. Karena wadah terbuka, maka sebagian kalor berpindah menuju udara.
Wadah juga menjadi lebih hangat. Kalor yang dilepaskan oleh air panas, tidak
hanya diserap oleh air dingin, tetapi juga diserap oleh udara dan wadah. Dalam
hal ini, wadah merupakan sistem tidak terisolasi.
Apabila kita mencampur air pans dan air dingin dalam
sebuah termos tertutup, maka terjadi perpindahan kalor dari air panas menuju
air dingin. Termos merupakan sistem terisolasi karenanya tidak ada kalor yang
berpindah menuju udara atau termos. Kalor yang dilepaskan oleh air panas hanya
diserap oleh air dingin hingga campuran air panas dan air dingin mencapai
kesetimbangan termal.
Asas Black menyatakan bahwa dalam sistem tertutup
terisolasi, kalor yang dilepaskan oleh benda bersuhu tinggi = kalor yang
diserap oleh benda bersuhu rendah.
Q lepas = Q serap
Untuk menentukan kalor jenis yang tidak diketahui dapat ditentukan
dengan menggunakan kalorimetri. Kalorimeter merupakan alat pengukuran
kuantitatif dari pertukaran kalor. Kalorimeter diisolasi dengan baik sehingga
hanya sejumlah minimum kalor yang dipertukarkan dengan luarnya. Teknik yang
dikenal sebagai “metode campuran”, satu sampel zat yang dipanaskan sampai
temperature tinggi yang diukur dengan akurat, dan dengan cepat ditempatkan pada
air dingin kalorimeter. Kalor yang hilang pada sampel tersebut akan diterima
oleh air dan calorimeter. Dengan mengukur temperature akhir campuran tersebut,
kalor jenis suatu zat dapat dihitung menggunakan hukum asas black.
Dimana indeks s, w dan kal mengacu pada sampel, air dan kalorimeter
berturut-turut
Kalor Laten (L)
Kalor dapat dibagi menjadi 2 jenis :
1.
Kalor yang digunakan untuk
menaikkan suhu
2.
Kalor yang digunakan untuk
mengubah wujud (kalor laten)
Ketika memasukkan
termometer raksa ke dalam sebuah wadah yang
berisi campuran
air dingin
dan es, maka setelah bergerak
ke bawah, permukaan raksa diam atau
tidak
bergerak lagi. Permukaan
raksa berhenti bergerak setelah mencapai suhu
titik lebur air atau titik
es atau
titik
beku air (0 oC). Jika wadah terbuka maka kalor mengalir dari udara bersuhu lebih tinggi menuju campuran es dan air yang bersuhu lebih rendah. Adanya tambahan kalor dari udara menyebabkan es mencair. Selama es
mencair, apakah
suhu campuran
es dan air
berubah? Selama es mencair, suhu campuran air dan es tidak berubah.
Apabila campuran
es dan air dipanaskan menggunakan
api atau
pemanas
listrik, misalnya, maka semua
es berubah menjadi
air. Jika terus
dipanaskan maka suhu air meningkat hingga mencapai
100 oC. Pada suhu 100 oC, air mulai menguap. Apabila nyala api diperbesar atau
air terus dipanaskan, semakin cepat air berubah
menjadi uap, sedangkan suhu air tidak mengalami perubahan atau tetap 100 oC. Ini adalah suhu titik didih air atau suhu tertinggi yang dapat dicapai
air.
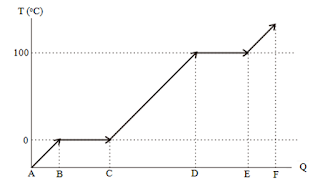
Grafik hubungan kalor
dengan perubahan suhu dan perubahan wujud air.
AB = Tambahan kalor menaikkan suhu es sampai
0 oC
BC = Tambahan kalor mencairkan es menjadi air
CD = Tambahan kalor
menaikkan suhu air dari
0 oC sampai
100
oC
DE = Tambahan kalor
menguapkan air
EF = Tambahan kalor menaikkan suhu uap
Grafik di atas
menunjukkan proses perubahan suhu
dan
perubahan wujud air selama air menyerap kalor (pada tekanan udara 1 atmosfer). Jika air melepaskan kalor maka proses yang terjadi adalah kebalikan dari
proses di atas
(tandah
panah di balik). Penambahan kalor dari B – C tidak menyebabkan
perubahan
suhu air tetapi hanya meleburkan
es
menjadi air. Demikian juga
penambahan kalor dari D – E tidak
menyebabkan
perubahan suhu air tetapi hanya mengubah air menjadi uap. Air hanya salah satu
contoh
saja. Pada dasarnya semua benda akan mengalami
proses perubahan wujud dan perubuhan suhu seperti
yang dialami
oleh air, jika benda tersebut
menyerap kalor. Perbedaannya terletak
pada titik beku
dan
titik didih. Setiap benda mempunyai titik beku dan titik didih yang berbeda. Jika benda melepaskan kalor
maka proses yang terjadi adalah kebalikan dari proses di
atas.
Persamaan yang digunakan dalam kalor
laten ada dua macam yaitu:
1.
Kalor Lebur
Kalor lebur adalah banyaknya kalor yang diserap oleh 1 kg benda
untuk mengubah wujudnya dari padat menjadi cair atau kalor yang dilepaskan 1 kg
benda untuk mengubah wujudnya dari cair menjadi padat.
Keterangan
: Q = kalor yang diserap atau dilepaskan (J), m = massa benda (kg), L = kalor
lebur (J/kg).
2.
Kalor Uap
Kalor uap adalah banyaknya kalor yang diserap oleh 1 kg benda
untuk mengubah wujudnya dari cair menjadi gas atau kalor yang dilepaskan 1 kg
benda untuk mengubah wujudnya dari gas menjadi cair.
Keterangan
: Q = kalor yang diserap atau dilepaskan (J), m = massa benda (kg), U = kalor
uap (J/kg)
Analisis grafik perubahan wujud pada es
yang dipanaskan sampai menjadi uap. Dalam grafik ini dapat dilihat semua
persamaan kalor digunakan.
Perpindahan Kalor
Kalor atau panas adalah energi yang
berpindah dari benda bersuhu tinggi menuju benda bersuhu rendah. Perpindahan
kalor terhenti setelah terjadi kesetimbangan termal. Jika anda mencampur air
panas dengan air dingin maka kalor berpindah dari air panas menuju air dingin.
Perpindahan kalor terhenti setelah terjadi kesetimbangan termal atau setelah
campuran air panas dan air dingin mencapai suhu yang sama.
Terdapat tiga jenis perpindahan kalor,
antara lain perpindahan kalor secara konduksi, perpindahan kalor secara
konveksi, perpindahan kalor secara radiasi.
1. Perpindahan kalor secara konduksi
Siapkan sebuah lilin
dan sepotong
kawat tipis. Pegang salah satu
ujung
kawat lalu sentuhkan ujung kawat lain ke
nyala
lilin. Tunggu selama
beberapa saat hingga
tanganmu kepanasan. Mengapa
tanganmu terasa panas ?
Ketika
salah
satu ujung kawat bersentuhan
dengan nyala lilin, kalor berpindah
dari nyala lilin
(suhu
tinggi) menuju
ujung kawat tersebut (suhu rendah). Adanya perpindahan kalor menyebabkan suhu
ujung kawat yang bersentuhan dengan api meningkat. Perbedaan suhu antara ujung kawat yang bersentuhan dengan nyala lilin dengan ujung kawat lainnya menyebabkan kalor berpindah dari ujung kawat yang
bersentuhan dengan api menuju
ujung kawat yang disentuh tangan. Adanya perpindahan
kalor menyebabkan
suhu ujung
kawat yang
disentuh
meningkat. Kalor
selanjutnya berpindah menuju tangan yang lebih dingin. Akibatnya tangan anda terasa panas.
Ketika salah satu
bagian
benda bersuhu tinggi bersentuhan
dengan benda
bersuhu
rendah, energi berpindah dari benda
bersuhu tinggi menuju
bagian
benda bersuhu rendah. Adanya tambahan energi menyebabkan atom dan
molekul penyusun benda bergerak semakin cepat. Ketika bergerak, molekul tersebut memiliki energi kinetik. Molekul-molekul yang bergerak lebih cepat (energi kinetiknya lebih besar) menumbuk molekul yang berada
di sebelahnya. Molekul tadi menumbuk
lagi molekul lain yang berada di sebelah. Demikian seterusnya. Jadi molekul-molekul saling bertumbukan, sambil
memindahkan energi. Perpindahan kalor yang terjadi melalui tumbukan antara molekul
pernyusun benda dinamakan perpindahan kalor secara konduksi.
 |
Berdasarkan hasil
percobaan,
kalor yang
berpindah selama
selang
waktu tertentu (Q/t) berbanding lurus dengan perbedaan suhu (T1–T2), luas penampang (A), sifat suatu benda (k =
konduktivitas termal) dan berbanding terbalik dengan panjang benda. Rumus laju perpindahan kalor
secara konduksi
:
Keterangan : Q/t = laju perpindahan kalor, k = konduktivitas termal, A = luas penampang, T1 = suhu tinggi, T2 = suhu rendah, l
= panjang benda.
2.
Perpindahan kalor secara konveksi
Perpindahan kalor secara
konduksi biasanya terjadi pada benda
padat atau
dari benda padat ke benda
cair (benda cair ke benda padat) atau dari
benda padat
ke
benda gas (benda gas ke benda padat). Sedangkan perpindahan kalor
secara konveksi
biasanya terjadi pada benda cair (misalnya air) dan benda gas
(misalnya udara).
Perpindahan kalor secara
konveksi adalah
perpindahan kalor yang disertai dengan
perpindahan
benda. Contoh perpindahan kalor secara konveksi misalnya
terjadi pada air yang dipanaskan
menggunakan api. Ketika air di dalam sebuah wadah
dipanaskan
dengan api, kalor berpindah
dari api (suhu tinggi) ke
wadah
(suhu
rendah) secara konduksi dan radiasi. Selanjutnya
kalor berpindah dari wadah (suhu lebih tinggi) ke air yang berada di dekat wadah (suhu lebih rendah) secara konduksi. Adanya tambahan kalor
menyebabkan suhu air
yang
berada di dekat wadah meningkat. Meningkatnya suhu air mengakibatkan air memuai atau volume air
bertambah. Karena volume
air bertambah maka massa
jenis
air berkurang. Air yang berada
di dekat alas
wadah mempunyai suhu lebih tinggi dibandingkan dengan air yang berada
di sebelah atasnya. Dengan
kata lain, air yang
berada di dekat alas wadah mempunyai volume lebih besar dan massa jenisnya lebih kecil, sedangkan air yang
berada di sebelah
atasnya mempunyai volume lebih kecil dan massa
jenisnya lebih besar. Adanya
perbedaan massa jenis
menyebabkan
air yang
berada di permukaan wadah, yang mempunyai massa
jenis lebih besar, bergerak ke
bawah dan air yang berada di dekat alas wadah, yang mempunyai massa jenis lebih kecil, bergerak ke atas. Proses ini terjadi secara terus menerus hingga semua air yang berada di dalam mempunyai suhu yang sama (Jika tekanan
udara 1 atmosfer maka air
di dalam wadah mengalami
penguapan alias mendidih pada suhu 100 oC).
Terjadinya angin darat dan angin laut juga melibatkan perpindahan kalor secara konduksi dan konveksi. Kalor jenis daratan (kalor jenis benda padat) lebih kecil daripada kalor jenis air laut, karenanya daratan lebih cepat panas ketika disinari matahari dan juga lebih cepat dingin ketika malam hari tiba. Daratan yang lebih cepat panas, memanaskan udara yang berada di atas (kalor berpindah dari daratan ke udara secara konduksi). Suhu udara yang mendapat tambahan kalor meningkat dan udara memuai. Akibatnya massa jenis udara tersebut berkurang. Sebaliknya suhu air laut lebih dingin sehingga udara yang berada di atas permukaan air laut juga lebih dingin, dibandingkan udara yang berada di permukaan daratan. Udara di permukaan laut lebih dingin sehingga massa jenisnya lebih besar. Adanya perbedaan massa jenis udara menyebabkan udara yang berada di permukaan laut bergerak menuju daratan dan menekan udara di daratan ke atas. Semakin jauh dari permukaan bumi, jumlah udara semakin berkurang karena gaya gravitasi bumi semakin kecil. Karena jumlah udara semakin berkurang maka tekanan udara juga semakin kecil. Udara panas di daratan yang bergerak ke atas mengalami pendinginan karena semakin jauh dari permukaan bumi, tekanan udara semakin berkurang. Udara dingin tersebut kemudian bergerak lagi ke bawah, tidak menuju permukaan daratan tetapi menuju permukaan lautan yang mempunyai suhu yang lebih dingin. Proses ini terjadi secara terus menerus sehingga timbul aliran udara dari laut menuju darat
3. Perpindahan kalor secara radiasi
Konduksi dan konveksi
memerlukan adanya materi sebagai medium untuk membawa kalor dari daerah yang
lebih panas ke yang lebih dingin. Tetapi perpindahan kalor secara radiasi
terjadi tanpa memerlukan medium apupun dan dalam bentuk gelombang elektromagnetik. Contoh
perpindahan kalor secara radiasi adalah
hangatnya tubuh anda ketika
berada
di dekat tungku api dan perpindahan kalor dari
matahari
menuju bumi. Matahari
memiliki suhu lebih tinggi (sekitar
6000 Kelvin), sedangkan
bumi memiliki suhu yang lebih rendah. Adanya
perbedaan
suhu antara matahari dan bumi menyebabkan
kalor berpindah
dari matahari (suhu lebih tinggi) menuju bumi (suhu lebih rendah). Seandainya perpindahan kalor dari matahari menuju
bumi memerlukan
perantara
alias medium, sebagaimana perpindahan
kalor secara konduksi dan konveksi, maka kalor tidak mungkin tiba di bumi. kalor harus melewati ruang hampa (atau hampir hampa). Jika tidak ada sumbangan kalor dari matahari, maka kehidupan di bumi tidak akan pernah ada karena kehidupan
membutuhkan energi.
Laju perpindahan kalor dengan cara radiasi ditemukan sebanding
dengan luas benda dan pangkat empat suhu mutlak (Skala Kelvin) benda tersebut.
Benda yang memiliki luas permukaan yang lebih besar memiliki laju perpindahan
kalor yang lebih besar dibandingkan dengan benda yang memiliki luas permukaan
yang lebih kecil.
Keterangan :
Q/t = laju perpindahan
kalor secara radiasi atau laju radiasi energi
A = Luas permukaan
benda (m2)
T = Suhu mutlak benda (K)
e =
Emisivitas (angka tak
berdimensi yang besarnya
berkisar antara 0 sampai
1),
σ = konstanta
Stefan-Boltzmann (5,67 x 10-8 W/m2.K4)











0 komentar:
Posting Komentar